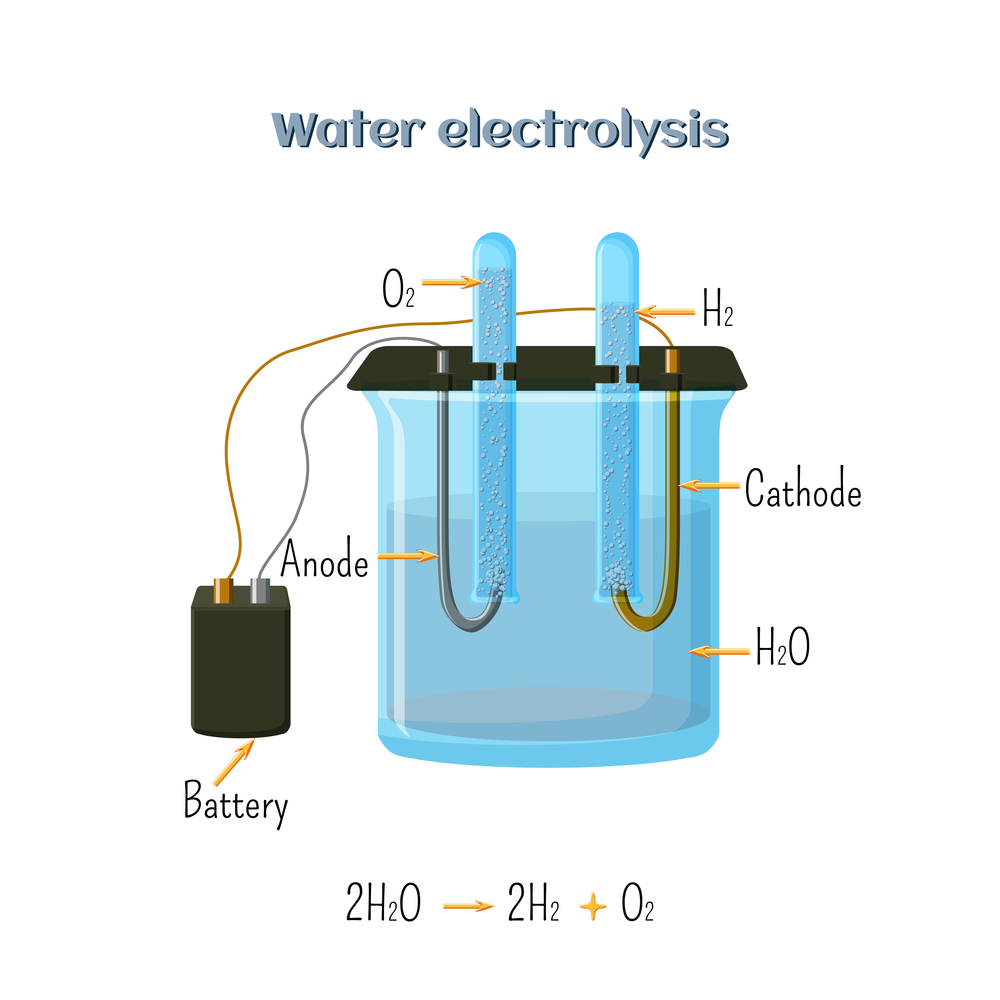
Water electrolysis diagram. Educational chemistry for kids. Source of hydrogen - alternative fuel. Cartoon vector illustration in flat style.
Que es la Electrolisis y para que se usa?
La electrólisis es un proceso electroquímico que utiliza corriente eléctrica para inducir una reacción química no espontánea. Ocurre en una celda electrolítica, que tiene dos electrodos (ánodo y cátodo) en un electrolito.
Componentes de la Celda Electrolítica:
– Ánodo: Electrodo positivo donde ocurre la oxidación.
– Cátodo: Electrodo negativo donde ocurre la reducción.
– Electrolito: Solución iónica que permite el flujo de iones.
Reacciones:
– Oxidación (Ánodo): M → Mn+ + ne−
– Reducción (Cátodo): Mn+ + ne− → M
Aplicaciones:
1. Producción de Metales: Extracción y purificación de metales, como la producción de aluminio.
2. Electrochapado: Depósito de una capa de metal sobre otro material.
3. Producción de Cloro y Soda Cáustica: Electroquímica de cloruro de sodio para obtener cloro e hidróxido de sodio.
4. Electrólisis del Agua: Descomposición de agua en oxígeno e hidrógeno para obtener energía limpia.
Ejemplos Prácticos:
1. Electrólisis del Agua: Celda con electrodos de platino o acero inoxidable y electrolito de KOH.
2. Purificación del Cobre: Transferencia de cobre del ánodo impuro al cátodo puro.
La electrólisis es esencial en la industria y la ciencia para producir metales, químicos y energía limpia, impulsando el avance tecnológico y la sostenibilidad.




